[生存戰場] 臨床試驗的神秘面紗
畢業後,大部分的人都會面臨「找工作」這件人生大事。接著,在逢年過節的時刻,總會有一兩位賊頭賊腦又不太熟的親戚,想辦法打聽你的近況,試圖噓寒問暖或冷嘲熱諷一番。
「阿安莉絲是不是今年畢業了啊?有沒有找到工作,薪水呢?該不會是 22K 吧?」
「喔,我只知道他在一家公司上班啦,好像做什麼臨床實驗的吧,老實說我也不太清楚我女兒到底在幹嘛。」
是的,大部分的人都不知道我們這一行在幹嘛,連我爸媽也不清楚,無從與親戚解釋。就這樣,我的工作一直是個謎,反正不是販毒詐騙搶劫等等不合法的事情,大概也沒人關心。(或者他們關心的只是薪水 XDD)
大部分醫學院的學生畢業之後,都會考國考,然後成為臨床執業人員。例如平常與大家最有接觸的醫師、護理師、藥師、物理治療師以及一定要提及的醫檢師 (沒有為什麼,因為我是醫技系畢業的)。再來,另一部分的人會投入生技慘業,大部分以新創公司居多,職位多與研發相關。也有一部分厲害的同學會進入藥廠,成為在醫院裡穿梭的一群 Propa。最後,還有一個選擇,稱為臨床試驗公司。
何謂臨床試驗?
絕對不是做實驗!!!!這是必須要澄清的一點,我們絕對不是拿病人來做實驗。請千萬別誤會我們是一群不人道的人,受試者的健康是我們最重視的事情。
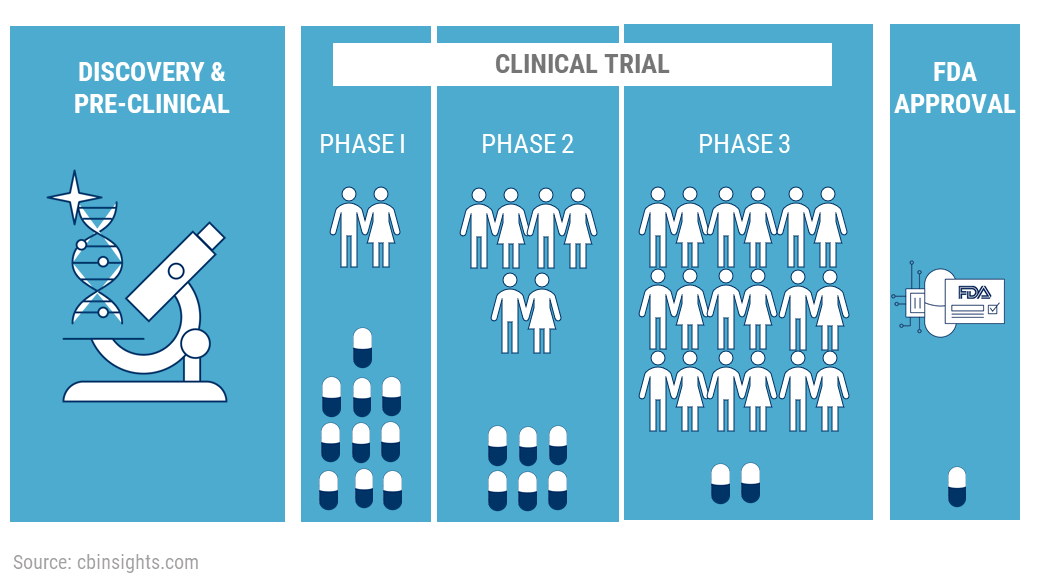
臨床試驗是新藥/新醫學技術/新醫材上市前必須經過的一個非常漫長的旅程。以我主要負責的按癌症標靶藥物來說,完整走完整個臨床試驗的時間大概是十年,所需要投入的金額是個天文數字,多道我算不出來有幾個零,我大概一輩子都沒辦法賺那麼多。
在執行試驗的這十年間,會相遇的人們大概可以分成幾個角色,分別為:
- 醫療行為執行:包含醫師、研究護理師、藥師等等
- 法規審核:台灣食藥署 (TFDA)、 醫院倫理研究委員會 (IRB)
- 試驗委託者:藥廠/生技廠
- 臨床試驗監測:臨床研究公司 (CRO)
舉例來說,藥廠研發藥物成功,完成動物實驗且要進階到人體試驗時,他們就會決定要合作的醫師團隊,且在試驗開始前必須提供受試者同意書與試驗計畫書給 TFDA 與 IRB 審核 (當然不止這兩項,還有很多文件要準備QQ)。在這嚴謹的審核過程當中,委員會對整個試驗過程全面的了解,並針對有疑慮的地方提出疑問。順利通過後,醫師便可以開始收案 (收病人),向符合收案標準的病人清楚的解釋整個試驗過程。病人完全理解且同意並簽下受試者同意書後,才可以開始進行療程,在這過程中,只要病人不想繼續療程,不需要任何理由即可退出試驗。
以我所在的CRO來說,我們會負責整個試驗過程的品質監測,透過臨床試驗專員 (CRA) 定期到醫院端訪視,確認一切都好。因為是人體研究,所以所有的資料都必須要好好的且正確的留存,確保病人的用藥安全且確認所有醫療行為都有遵照試驗計畫書執行,就是 CRA 們最主要的工作之一 (我講的很簡略,但實際上這是一份相當偉大的工作)。

等到試驗完成,也就是病人的療程與追蹤全部都結束之後,就會將其中得到的資料進行分析,等待分析結果 (也就是前一陣子很紅的「合一解盲成功」事件)。如果到這邊都成功,就可以接下來的新藥上市審查,發大財之路就此展開。'
光是簡單的皮毛講解,就成就了我這一篇文章。這真的只是皮毛中的皮毛,我剛入行不久,也還有很多要學習的地方。所以,我就索性不與親戚們解釋我到底在幹嘛了。
其實我覺得,所以醫學相關從業人員,大家都會有一顆想要幫助人類的心。即使多年的摧殘過去,我們在面對那些動粗的病人、醫院評鑑的荒唐、一言難盡的健保制度、道不盡的壓力與委屈時,或許大家都曾在夜深人靜時默默流下那麼一滴淚,但支持我們走下去的,就是病人康復後的笑容、新藥上市後的興奮。也許我們再也回不到當年畢業時的那種滿腔熱血,但每個人的心中,仍有一塊淨土,裝載了想要為社會做點什麼的心意。
願我們都能在自己的崗位上繼續貢獻自我,當然也不需要到燃燒生命廢寢忘食的程度,還是要記得吃飯喝水上廁所。
All the best.
